Neurally Adjusted Ventilatory Assist nel neonato
Ventilare un neonato prematuro ricercando la migliore strategia di sincronizzazione rappresenta una sfida quotidiana in neonatologia. Il tempo inspiratorio particolarmente breve, i bassi volumi correnti, le elevate frequenze respiratorie e la presenza di perdite legate all’utilizzo di tubi non cuffiati e interfacce non invasive esclusivamente nasali comportano numerose difficoltà nella sincronizzazione, tanto da limitare l’utilizzo di ventilazioni sincronizzate in quest’ambito.
Il prevalente utilizzo di modalità di ventilazione non sincronizzate comporta, naturalmente, un alto tasso di eventi asincroni, con un’incidenza di asincronie paziente – ventilatore che variano, in neonatologia, dal 45% al 68% 1,2. Un alto tasso di asincronie comporta, per il neonato pretermine, un’aumentata esposizione a barotrauma, rischio di pneumotorace ma anche emorragia intraventricolare3 ed un enorme dispendio energetico determinato dall’esigenza di “combattere” il ventilatore; crescenti evidenze sottolineano come il discomfort derivante dalle procedure e dai trattamenti, e tra questi anche la ventilazione meccanica, possano impattare negativamente sugli outcome neurologici a breve e lungo termine del neonato4,5.
Neurally Adjusted Ventilatory Assist (NAVA) è un’innovativa modalità di ventilazione proporzionale che sfrutta l’attività elettrica diaframmatica per sincronizzare il supporto della macchina al respiro del paziente istante per istante. A questa peculiare caratteristica definente di NAVA, si integra la modulazione della ventilazione sulla base dei riflessi protettivi polmonari, che intervengono regolando l’attività diaframmatica sulla base del grado di stiramento polmonare, favorendo così una ventilazione personalizzata e meno lesiva per il polmone ed il diaframma. Questa modalità rappresenta una potenziale soluzione alla difficoltà di sincronizzazione nella ventilazione neonatale.
Le evidenze dimostrano che, nel neonato, NAVA garantisce la miglior sincronizzazione possibile migliorando l’interazione paziente – ventilatore1,6–8; NAVA migliora inoltre il comfort riducendo la necessità di sedazione9,10, la pressione inspiratoria di picco (PIP)6–8,11, il fabbisogno di FiO26–8, le apnee centrali12 e sembra ridurre il tasso di fallimento dell’estubazione rispetto alla nCPAP13 e alla NIPPV14,15. Quel che ancora non è chiaro in letteratura è se l’utilizzo di NAVA possa concretamente ridurre i giorni di ventilazione meccanica nella popolazione neonatale e se possa realmente avere un effetto protettivo sul diaframma.
Per garantire un’adeguata assistenza ed un adeguato trattamento al paziente in NAVA è fondamentale conoscere il significato del monitoraggio dell’attività elettrica diaframmatica (Edi o EAdi).
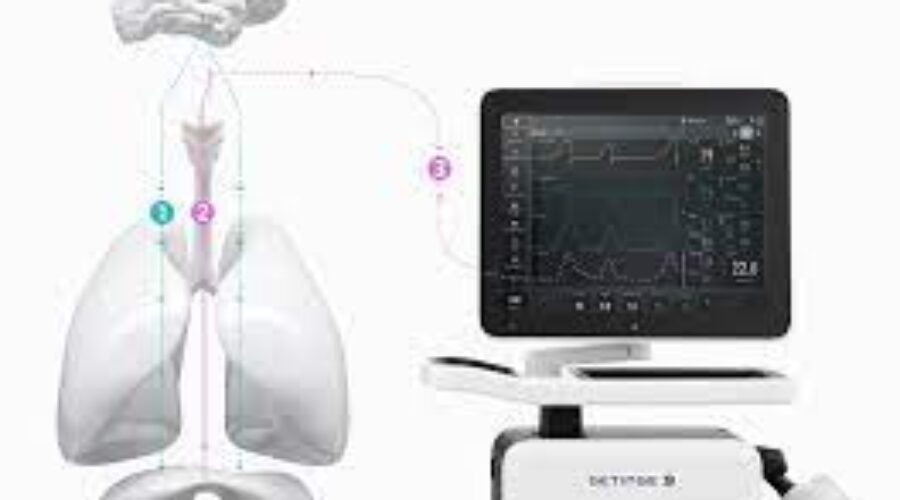
Il catetere Edi è lo strumento che permette al ventilatore di sincronizzarsi con l’attività elettrica diaframmatica, attraverso elettrodi contenuti in un sondino gastrico che vengono posizionati in prossimità del diaframma (figura 1). Questo strumento permette di ridurre al minimo il periodo di latenza tra l’intercettazione dello sforzo respiratorio del paziente e l’erogazione del supporto ventilatorio e permette, inoltre, di monitorare accuratamente la funzione diaframmatica. Conoscere i fondamenti del monitoraggio Edi è dunque essenziale nel monitoraggio bedside.

Figura 1: posizione del catetere Edi, da notare la matrice di elettrodi, posizionata nella parte terminale del sondino, a cavallo del diaframma. Immagine tratta da Bulleri E, Fusi C. Guida al monitoraggio della ventilazione meccanica, Triggerlab, 2020.
Setting e monitoraggio
Il grado di eccitazione diaframmatica espresso in μV rilevato dal catetere Edi è utilizzato per due scopi:
- impostare la soglia del trigger neurale (Figura 2), teoricamente più sensibile dei sistemi tradizionali;
- regolare il livello di supporto inspiratorio (livello NAVA).
Il livello NAVA determina la proporzionalità tra il segnale Edi ed il supporto pressorio erogato dal ventilatore. L’operatore imposta quindi il livello di PEEP e la FiO2, ma non la pressione inspiratoria, che sarà invece determinata dal livello NAVA in funzione del livello di attivazione elettrica diaframmatica (segnale Edi). Il livello NAVA esprime dunque quanti cmH2O il paziente riceverà per μV di depolarizzazione diaframmatica istante per istante (Figura 3).

Figura 2: curva di depolarizzazione del diaframma misurata attraverso il catetere Edi. Da notare il livello di trigger impostato sopra Edi min (attivita elettrica basale).

Figura 3: la quantità di pressione erogata (in cm H2O) viene regolata moltiplicando l’Edi (che è espresso in μV) per un fattore di proporzionalità, il “livello NAVA” (espresso come cm H2O/μV). Ad esempio, quando il catetere Edi misura una depolarizzazione di 10 μV, un livello NAVA di 2 cmH2O/μV darà 20 cmH2O.
La pressione inspiratoria di picco è infatti il risultato della seguente equazione:
PIP = NAVA level x (EdiPeak – EdiMin) + PEEP
Il livello NAVA può essere scelto in funzione del comfort del paziente, mantenendo un livello di EdiPeak intorno ai 10-15 μV, oppure prendendo come riferimento la pressione inspiratoria applicata che si vuole raggiungere16.
Se scegliamo come target una pressione inspiratoria sopra PEEP di 10 cmH2O ed abbiamo un Edi Peak 14μV ed un EdiMin 2μV, il calcolo per ottenere il NAVA level è il seguente:
NAVA level = 10 cmH2O/(14 μV-2 μV) = 0.8 cmH2O/μV
Una volta settata la ventilazione, fondamentale nella gestione del paziente in NAVA è il monitoraggio del segnale Edi. Il segnale Edi è infatti in grado di guidare l’operatore nella gestione delle modifiche da apportare ai parametri ventilatori.
Le evidenze dimostrano che in neonati in respiro spontaneo EdiPeak si attesta intorno ai 10 – 11μV , mentre EdiMin intorno ai 2 – 3 μV 16–18. In neonati ventilati, EdiPeak ed EdiMin rappresentano due parametri fondamentali per le decisioni cliniche:
- EdiPeak > 20 μV in neonati ventilati è indicativo di aumentato lavoro respiratorio; il primo elemento da considerare quando viene rilevato un livello EdiPeak alto è il corretto posizionamento del sondino Edi, al fine di escludere qualsiasi tipo di errore di posizionamento e dunque interferenze al monitoraggio. Se il sondino è correttamente posizionato, questa condizione può essere il risultato di un livello NAVA troppo basso, discomfort o dolore o, ancora, di un’inadeguata ventilazione di backup (ricordiamo che l’immaturità dei centri del respiro del neonato induce episodi di apnea centrale tanto più frequenti quanto più bassa è l’età gestazionale; un buon settaggio dei tempi di apnea e della ventilazione di backup è fondamentale in questi pazienti)16,19–23,26.
- EdiPeak <5 μV in neonati ventilati può essere indicativo di un eccessivo supporto da parte della macchina; livelli NAVA troppo elevati per il paziente possono ridurre la sua attività spontanea poiché sovra-assistito. Il diaframma tende, in questo frangente, a lavorare sempre meno poiché la maggior parte del lavoro viene svolta dalla macchina; a lungo andare, una sovra-assistenza può indurre un’atrofia diaframmatica24,26.
- EdiMin persistentemente > 5μV può essere un segnale indicativo di atelettasia. EdiMin rappresenta l’attività elettrica di contrazione tonica del diaframma, ovvero il grado di contrazione a riposo. Sappiamo che il diaframma non è mai completamente a riposo ed in particolar modo nel neonato, in cui il rapporto tra la compliance della gabbia toracica e la compliance polmonare è particolarmente elevato, il grado di contrazione a riposo è maggiore rispetto all’adulto. La contrazione tonica è l’espressione del tentativo del diaframma di garantire una capacità funzionale residua polmonare. L’aumento di questo grado di contrazione è dunque espressione della maggior attività elettrica del diaframma a riposo in caso di presenza di zone atelettasiche19,22,23,26.
Tempo di apnea
A causa dell’immaturità del sistema nervoso centrale e dei centri del respiro del neonato pretermine, multipli episodi di apnea possono verificarsi durante la ventilazione e la loro incidenza risulta essere strettamente correlata al grado di immaturità. Questa immaturità determina un’alta variabilità nel pattern respiratorio del neonato, fattore che spesso induce l’operatore a cambiare modalità di ventilazione per passare ad una non sincronizzata intermittente.
La scelta di un adeguato tempo di apnea è cruciale durante la ventilazione in NAVA, poiché permette al neonato di non essere sovra-assistito e di stabilire una frequenza respiratoria spontanea minima senza l’intervento del ventilatore qualora non necessario; la fisiologica variabilità del pattern respiratorio del neonato induce infatti il ventilatore ad intervenire frequentemente con una ventilazione di backup qualora venga impostato un tempo di apnea troppo breve. La letteratura suggerisce di iniziare con un tempo di apnea di 2 secondi nei neonati con età gestazionale inferiore alle 30 settimane e di aumentare progressivamente con la crescita e la maturazione25.
Il tempo di apnea può inoltre rappresentare un utile ausilio in fase di weaning del neonato pretermine, da interpretare come indicatore della maturità dei centri del respiro. L’allungamento di questo tempo ci permette infatti di comprendere quanto il neonato sia in grado di ventilare autonomamente senza la periodica necessità di intervenire con una ventilazione di backup. Il raggiungimento di un tempo di apnea di 5 secondi è considerato indicativo di prontezza al weaning25
Fonte :